Phác đồ chẩn đoán và điều trị lao phổi
THƯ VIỆN MEDIPHARM
1. Đại cương
1.1. Định nghĩa
Lao phổi là bệnh nhiễm trùng do vi khuẩn Mycobacterium tuberculosis gây ra, chủ yếu ảnh hưởng đến phổi. Bệnh có thể lây truyền từ người sang người qua đường hô hấp và có khả năng gây tổn thương nghiêm trọng đến cơ quan hô hấp nếu không được điều trị kịp thời và đúng cách.
1.2. Dịch tễ học
- Theo WHO (2021), có khoảng 10 triệu ca mắc mới và 1,5 triệu ca tử vong do lao trên toàn cầu.
- Tỷ lệ mắc cao nhất ở Đông Nam Á, châu Phi và Tây Thái Bình Dương.
- Các yếu tố nguy cơ: HIV/AIDS, suy dinh dưỡng, tiểu đường, hút thuốc lá, lạm dụng rượu.
1.3. Tác nhân gây bệnh
- Mycobacterium tuberculosis complex, bao gồm:
- M. tuberculosis (phổ biến nhất ở người)
- M. bovis (chủ yếu ở động vật, hiếm gặp ở người)
- M. africanum (chủ yếu ở Tây Phi)
- Đặc điểm vi khuẩn:
- Trực khuẩn ưa khí, không di động, không sinh bào tử
- Kích thước 0.3-0.6 x 1-4 μm
- Tồn tại lâu trong môi trường, nhạy cảm với tia cực tím
Đặc điểm Vi khuẩn lao:
- Hình thái học:
- Trực khuẩn thẳng hoặc hơi cong
- Kích thước: 0.3-0.6 μm x 1-4 μm
- Không di động, không sinh bào tử
- Đặc tính sinh hóa:
- Ưa khí bắt buộc
- Kháng acid do thành tế bào chứa nhiều lipid
- Nhuộm Ziehl-Neelsen hoặc huỳnh quang auramine
- Đặc điểm nuôi cấy:
- Phát triển chậm: thời gian phân chia khoảng 15-20 giờ
- Môi trường nuôi cấy đặc: Löwenstein-Jensen, Middlebrook 7H10
- Môi trường nuôi cấy lỏng: MGIT (Mycobacteria Growth Indicator Tube)
- Đặc tính kháng thuốc:
- Kháng thuốc tự nhiên do cấu trúc thành tế bào đặc biệt
- Khả năng phát triển kháng thuốc mắc phải thông qua đột biến
- Gen và hệ gen:
- Kích thước hệ gen khoảng 4.4 Mb
- Giàu guanine và cytosine (65%)
- Có nhiều gen liên quan đến tổng hợp lipid và điều hòa chuyển hóa
1.4. Đường lây truyền
- Chủ yếu qua đường hô hấp, từ người bệnh lao phổi AFB dương tính sang người lành qua các giọt bắn có chứa vi khuẩn.
- Các yếu tố ảnh hưởng đến khả năng lây truyền:
- Số lượng vi khuẩn trong đờm
- Mức độ ho của người bệnh
- Thời gian và mức độ tiếp xúc
- Điều kiện môi trường (không gian kín, thiếu thông gió)
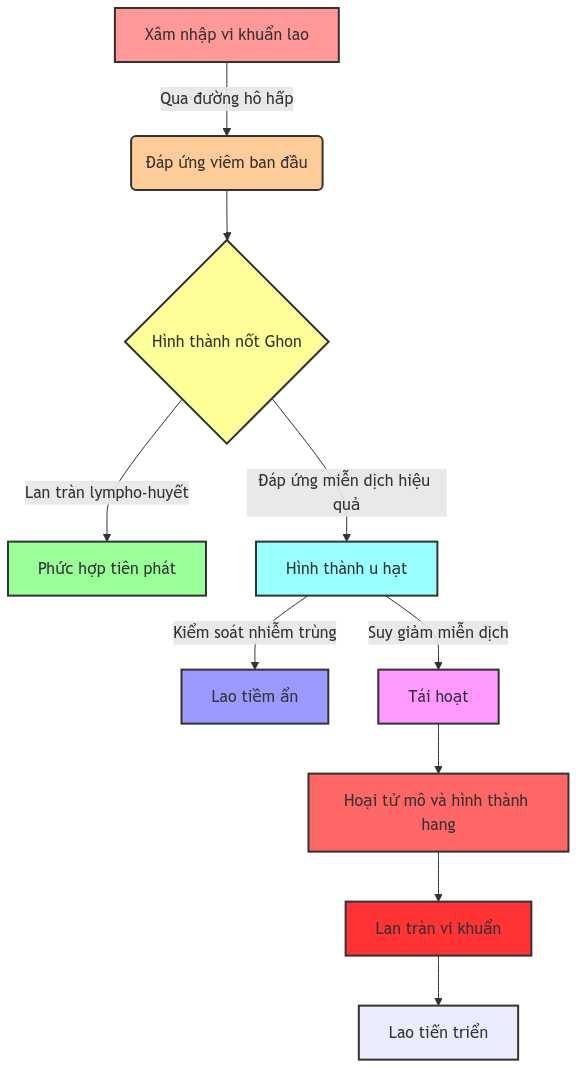
1.5. Cơ chế bệnh sinh và sinh lý bệnh
1.5.1. Giai đoạn xâm nhập và nhiễm trùng ban đầu
- Xâm nhập:
- Vi khuẩn lao xâm nhập vào phổi qua đường hô hấp
- Các hạt khí dung chứa vi khuẩn (kích thước 1-5 μm) đi qua đường thở và đến phế nang
- Đáp ứng viêm ban đầu:
- Đại thực bào phế nang nhận diện và nuốt vi khuẩn
- Tiết ra các cytokine gây viêm (TNF-α, IL-1, IL-6)
- Thu hút bạch cầu trung tính và tế bào lympho đến vùng nhiễm trùng
- Hình thành nốt Ghon:
- Tập trung các đại thực bào nhiễm khuẩn và tế bào viêm
- Hình thành tổn thương đặc trưng gọi là nốt Ghon
1.5.2. Giai đoạn lan tràn và hình thành phức hợp tiên phát
- Lan tràn lympho-huyết:
- Vi khuẩn lan tràn qua hệ bạch huyết đến hạch lympho vùng rốn phổi
- Có thể lan tràn qua máu đến các cơ quan khác
- Hình thành phức hợp tiên phát:
- Nốt Ghon + đường dẫn lympho bị viêm + hạch rốn phổi sưng to
- Đặc trưng cho lao tiên phát ở trẻ em và người suy giảm miễn dịch
1.5.3. Giai đoạn kiểm soát nhiễm trùng và hình thành u hạt
- Đáp ứng miễn dịch tế bào:
- Tế bào T CD4+ và CD8+ được hoạt hóa
- Tiết interferon-γ (IFN-γ) kích thích đại thực bào
- Hình thành u hạt:
- Đại thực bào hoạt hóa (tế bào bọt) tập trung quanh vi khuẩn
- Tế bào lympho T và B bao quanh
- Hình thành lớp tế bào xơ bên ngoài
- Kiểm soát nhiễm trùng:
- U hạt giúp cô lập và kiểm soát sự nhân lên của vi khuẩn
- Phần lớn vi khuẩn bị tiêu diệt hoặc ở trạng thái ngủ
1.5.4. Giai đoạn tiến triển bệnh (ở một số trường hợp)
- Sự tái hoạt của vi khuẩn:
- Do suy giảm miễn dịch hoặc các yếu tố khác
- Vi khuẩn tăng sinh nhanh chóng
- Hoại tử mô:
- U hạt bị phá vỡ, gây hoại tử mô phổi
- Hình thành hang lao
- Lan tràn vi khuẩn:
- Vi khuẩn lan tràn qua đường thở đến các vùng khác của phổi
- Có thể lan tràn qua máu đến các cơ quan khác (lao ngoài phổi)
1.5.5. Đáp ứng miễn dịch và tổn thương mô
- Đáp ứng miễn dịch quá mức:
- Giải phóng nhiều cytokine gây viêm
- Gây tổn thương mô phổi lan rộng
- Xơ hóa và canxi hóa:
- Quá trình lành thương dẫn đến xơ hóa mô phổi
- Các tổn thương cũ có thể bị canxi hóa
2. Chẩn đoán
2.1. Lâm sàng
2.1.1. Triệu chứng hô hấp
- Ho kéo dài: Trên 2-3 tuần, thường khan hoặc có đờm
- Ho ra máu: Từ ít đến nhiều, màu đỏ tươi hoặc đỏ sẫm
- Khó thở: Thường xuất hiện ở giai đoạn muộn hoặc khi có tràn dịch màng phổi
- Đau ngực: Có thể do tổn thương nhu mô phổi hoặc màng phổi
2.1.2. Triệu chứng toàn thân
- Sốt: Thường sốt nhẹ về chiều, có thể kèm ra mồ hôi đêm
- Gầy sút cân: Giảm >5% trọng lượng cơ thể trong vòng 6 tháng
- Mệt mỏi, chán ăn
- Ra mồ hôi đêm: Thường xảy ra vào nửa đêm về sáng
2.1.3. Khám thực thể
- Khám phổi: Có thể nghe thấy ran nổ, ran ẩm, hoặc hội chứng đông đặc
- Khám hạch: Có thể sờ thấy hạch to ở vùng cổ, nách, bẹn
- Dấu hiệu suy mòn: Giảm khối cơ, da xanh, niêm mạc nhợt
2.2. Cận lâm sàng
2.2.1. Xét nghiệm vi sinh
a) Soi trực tiếp tìm AFB (Acid-Fast Bacilli):
- Phương pháp nhuộm Ziehl-Neelsen hoặc huỳnh quang
- Độ nhạy: 50-60% ở bệnh nhân lao phổi AFB dương tính
- Ưu điểm: Nhanh, rẻ; Nhược điểm: Độ nhạy thấp
b) Nuôi cấy:
- Môi trường đặc Löwenstein-Jensen hoặc môi trường lỏng MGIT
- Độ nhạy: 80-85%, độ đặc hiệu: >98%
- Ưu điểm: Độ nhạy và đặc hiệu cao; Nhược điểm: Thời gian chờ kết quả lâu (2-8 tuần)
c) Xét nghiệm khuếch đại axit nucleic:
- Gen Xpert MTB/RIF: Phát hiện vi khuẩn lao và kháng Rifampicin
- Độ nhạy: >90% ở bệnh nhân AFB dương tính, 60-70% ở bệnh nhân AFB âm tính
- Độ đặc hiệu: >95%
- Ưu điểm: Nhanh (2 giờ), phát hiện kháng Rifampicin
d) Xét nghiệm Line Probe Assay (LPA):
- Phát hiện kháng đa thuốc (MDR-TB)
- Độ nhạy và độ đặc hiệu cao cho Isoniazid và Rifampicin
- Ưu điểm: Nhanh hơn nuôi cấy (1-2 ngày)
2.2.2. Chẩn đoán hình ảnh
a) X-quang phổi:
- Tổn thương thường gặp: Nốt, đám mờ, hang, xơ vôi hóa
- Vị trí: Thường ở thùy trên và đỉnh thùy dưới
- Độ nhạy cao nhưng độ đặc hiệu thấp
b) CT scan ngực:
- Phát hiện tổn thương sớm và chi tiết hơn X-quang
- Hữu ích trong đánh giá biến chứng và theo dõi điều trị
- Chỉ định: Khi X-quang không rõ ràng hoặc nghi ngờ biến chứng
c) PET-CT:
- Có thể giúp phân biệt tổn thương hoạt động và không hoạt động
- Hữu ích trong theo dõi đáp ứng điều trị
- Chỉ định hạn chế do chi phí cao
2.2.3. Xét nghiệm miễn dịch
a) Test Mantoux (TST):
- Tiêm 0.1 ml PPD trong da, đọc kết quả sau 48-72 giờ
- Dương tính khi đường kính cứng >10mm (hoặc >5mm ở người suy giảm miễn dịch)
- Độ nhạy và đặc hiệu không cao, có thể dương tính giả do tiêm BCG
b) Interferon-Gamma Release Assay (IGRA):
- QuantiFERON-TB Gold hoặc T-SPOT.TB
- Độ đặc hiệu cao hơn TST, không bị ảnh hưởng bởi tiêm BCG
- Ưu điểm: Không cần tái khám để đọc kết quả
- Nhược điểm: Chi phí cao, không phân biệt được lao tiềm ẩn và lao hoạt động
2.2.4. Xét nghiệm máu
- Công thức máu: Có thể thấy thiếu máu, tăng bạch cầu
- CRP và tốc độ lắng máu: Thường tăng
- Chức năng gan (AST, ALT, bilirubin): Đánh giá trước và trong quá trình điều trị
- Chức năng thận (ure, creatinin): Đánh giá trước khi dùng thuốc đào thải qua thận
- HIV: Xét nghiệm HIV cho tất cả bệnh nhân nghi ngờ lao
2.2.5. Các xét nghiệm khác
- Nội soi phế quản: Lấy mẫu bệnh phẩm ở bệnh nhân không khạc được đờm
- Sinh thiết hạch, màng phổi: Khi nghi ngờ lao ngoài phổi kèm theo
- Chọc dò dịch màng phổi: Xét nghiệm tế bào, sinh hóa, AFB và nuôi cấy
2.3. Chẩn đoán xác định
Chẩn đoán xác định lao phổi dựa trên sự kết hợp của:
- Triệu chứng lâm sàng gợi ý
- VÀ có ít nhất một trong các tiêu chuẩn sau:
- Soi đờm trực tiếp (+) với AFB
- Nuôi cấy (+) với M. tuberculosis
- Xét nghiệm Gen Xpert MTB/RIF (+)
- HOẶC có tổn thương nghi lao trên X-quang phổi và đáp ứng với điều trị lao
2.4. Chẩn đoán phân biệt
| Bệnh | Đặc điểm phân biệt |
|---|---|
| Viêm phổi do vi khuẩn | Khởi phát cấp tính, đáp ứng với kháng sinh thông thường |
| Ung thư phổi | Hình ảnh khối đặc trưng trên CT, xét nghiệm tế bào học |
| Bệnh phổi tắc nghẽn mạn tính (COPD) | Tiền sử hút thuốc, khó thở mạn tính, test hồi phục phế quản (+) |
| Nấm phổi | Thường ở bệnh nhân suy giảm miễn dịch, nuôi cấy nấm (+) |
| Viêm phổi kẽ | Hình ảnh CT đặc trưng, xét nghiệm AFB và nuôi cấy (-) |
2.5. Đánh giá mức độ nặng và biến chứng
- Lao phổi lan tỏa: Tổn thương >2/3 diện tích phổi trên X-quang
- Lao kê: Nhiều nốt nhỏ lan tỏa hai phổi
- Tràn dịch màng phổi: Đánh giá bằng X-quang, siêu âm hoặc CT ngực
- Tràn khí màng phổi: Có thể do vỡ hang lao
- Lao màng não: Đánh giá khi có triệu chứng thần kinh
- Lao hạch: Sờ và siêu âm hạch vùng cổ, nách, bẹn
2.6. Chẩn đoán lao kháng thuốc
- Nghi ngờ khi:
- Thất bại điều trị với phác đồ chuẩn
- Tái phát sau điều trị đủ
- Tiếp xúc với bệnh nhân lao kháng thuốc
- Xác định bằng:
- Gen Xpert MTB/RIF: Phát hiện kháng Rifampicin
- Xét nghiệm LPA: Phát hiện kháng Isoniazid và Rifampicin
- Kháng sinh đồ truyền thống: Xác định mức độ kháng với các thuốc khác
2.7. Chẩn đoán lao ở nhóm đặc biệt
2.7.1. Lao ở người nhiễm HIV
- Triệu chứng có thể không điển hình
- X-quang có thể có hình ảnh không đặc trưng
- Nên làm Gen Xpert MTB/RIF cho mọi bệnh nhân HIV nghi lao
2.7.2. Lao ở trẻ em
- Triệu chứng thường không đặc hiệu
- Khó lấy bệnh phẩm đờm
- Có thể dựa vào tiền sử tiếp xúc, TST, và hình ảnh X-quang
2.7.3. Lao ở người cao tuổi
- Triệu chứng có thể bị che lấp bởi các bệnh đồng mắc
- Cần chú ý phân biệt với các bệnh lý khác ở người cao tuổi
2.8. Theo dõi đáp ứng điều trị
- Lâm sàng: Đánh giá cải thiện triệu chứng
- Vi sinh: Xét nghiệm đờm AFB và nuôi cấy định kỳ
- X-quang: Đánh giá cải thiện tổn thương
- Cân nặng: Theo dõi tăng cân
3. Điều trị
3.1. Nguyên tắc điều trị
- Phối hợp nhiều thuốc: Để ngăn ngừa kháng thuốc và tăng hiệu quả điều trị.
- Điều trị đủ liều, đủ thời gian: Đảm bảo tiêu diệt hoàn toàn vi khuẩn.
- Điều trị có giám sát trực tiếp (DOT): Tăng tuân thủ điều trị.
- Điều trị sớm, liên tục: Ngăn ngừa biến chứng và lây lan.
- Cá thể hóa điều trị: Dựa trên tình trạng bệnh nhân và đặc điểm vi khuẩn.
3.2. Phác đồ điều trị
3.2.1. Lao mới, chưa điều trị
Phác đồ: 2HRZE/4HR (6 tháng)
a) Giai đoạn tấn công (2 tháng đầu):
- Isoniazid (H): 5 mg/kg/ngày (tối đa 300 mg)
- Rifampicin (R): 10 mg/kg/ngày (tối đa 600 mg)
- Pyrazinamide (Z): 25 mg/kg/ngày (tối đa 2000 mg)
- Ethambutol (E): 15-20 mg/kg/ngày (tối đa 1600 mg)
b) Giai đoạn duy trì (4 tháng tiếp):
- Isoniazid (H): 5 mg/kg/ngày (tối đa 300 mg)
- Rifampicin (R): 10 mg/kg/ngày (tối đa 600 mg)
Cách dùng:
- Uống một lần duy nhất vào buổi sáng, lúc đói
- Có thể dùng thuốc phối hợp liều cố định để tăng tuân thủ
Điều chỉnh liều:
- Với bệnh nhân >50 kg: Có thể tăng liều Rifampicin lên 750 mg/ngày
- Với bệnh nhân suy thận: Giảm liều Ethambutol và Pyrazinamide theo mức lọc cầu thận
3.2.2. Lao tái phát, thất bại, điều trị lại
Bắt buộc làm Gen Xpert MTB/RIF và kháng sinh đồ trước khi điều trị
a) Nếu nhạy với Rifampicin: 2HRZES/1HRZE/5HRE
- Giai đoạn tấn công 1: 2 tháng HRZES
- Giai đoạn tấn công 2: 1 tháng HRZE
- Giai đoạn duy trì: 5 tháng HRE
Liều lượng:
- Streptomycin (S): 15 mg/kg/ngày (tối đa 1000 mg), tiêm bắp hoặc tĩnh mạch
b) Nếu kháng Rifampicin: Chuyển phác đồ điều trị lao đa kháng thuốc
3.2.3. Lao đa kháng thuốc (MDR-TB)
Phác đồ chuẩn: 6 Bdq-Lfx-Lzd-Cfz-Cs / 14 Lfx-Lzd-Cfz-Cs
a) Giai đoạn tấn công (6 tháng):
- Bedaquiline (Bdq): 400 mg/ngày trong 2 tuần đầu, sau đó 200 mg 3 lần/tuần
- Levofloxacin (Lfx): 750-1000 mg/ngày
- Linezolid (Lzd): 600 mg/ngày
- Clofazimine (Cfz): 100 mg/ngày
- Cycloserine (Cs): 10-15 mg/kg/ngày (tối đa 1000 mg)
b) Giai đoạn duy trì (14 tháng):
- Levofloxacin (Lfx): 750-1000 mg/ngày
- Linezolid (Lzd): 600 mg/ngày
- Clofazimine (Cfz): 100 mg/ngày
- Cycloserine (Cs): 10-15 mg/kg/ngày (tối đa 1000 mg)
Thời gian điều trị: 18-20 tháng, có thể kéo dài đến 24 tháng tùy theo đáp ứng điều trị
Điều chỉnh phác đồ:
- Dựa trên kết quả kháng sinh đồ
- Có thể thêm thuốc như Delamanid, Pretomanid trong trường hợp kháng thuốc rộng
3.3. Điều trị hỗ trợ
- Corticosteroid:
- Chỉ định: Lao màng não, lao màng tim, lao phổi nặng với suy hô hấp
- Liều: Prednisone 1 mg/kg/ngày, giảm dần trong 6-8 tuần
- Pyridoxine (Vitamin B6):
- Chỉ định: Phòng ngừa độc tính thần kinh do Isoniazid
- Liều: 25-50 mg/ngày
- Dinh dưỡng:
- Chế độ ăn giàu protein, vitamin
- Bổ sung đa vitamin nếu cần
- Điều trị triệu chứng:
- Giảm đau: Paracetamol, NSAIDs nếu cần
- Ho: Thuốc giảm ho nếu ho nhiều ảnh hưởng giấc ngủ
3.4. Theo dõi và đánh giá điều trị
3.4.1. Lâm sàng
- Đánh giá hàng tháng: Cân nặng, triệu chứng ho, sốt, mệt mỏi
- Tìm tác dụng phụ của thuốc
3.4.2. Xét nghiệm
a) Xét nghiệm đờm:
- AFB trực tiếp và nuôi cấy: Tháng 0, 2, 5 và kết thúc điều trị
- Nếu vẫn dương tính ở tháng 2: Làm thêm kháng sinh đồ
b) X-quang phổi:
- Chụp ở tháng 0, 2 và kết thúc điều trị
- Chụp thêm nếu có diễn biến bất thường
c) Xét nghiệm chức năng gan:
- AST, ALT, bilirubin: Trước điều trị và mỗi tháng trong 3 tháng đầu
- Sau đó làm mỗi 3 tháng hoặc khi có triệu chứng
d) Xét nghiệm chức năng thận:
- Creatinin: Trước điều trị và mỗi tháng nếu dùng thuốc tiêm
e) Điện tâm đồ:
- Trước điều trị và mỗi tháng nếu dùng Bedaquiline hoặc Delamanid
f) Thị lực và phân biệt màu sắc:
- Kiểm tra hàng tháng nếu dùng Ethambutol
3.5. Xử trí tác dụng phụ
3.5.1. Độc tính gan
- Triệu chứng: Vàng da, buồn nôn, ALT >3 lần giới hạn trên
- Xử trí: Ngưng tất cả thuốc, theo dõi chức năng gan
- Tái sử dụng: Khi ALT <2 lần giới hạn trên, bắt đầu lại từng thuốc một
3.5.2. Phản ứng da
- Triệu chứng: Ngứa, phát ban
- Xử trí: Điều trị triệu chứng, nếu nặng ngưng thuốc và chuyển chuyên khoa
3.5.3. Viêm dây thần kinh ngoại biên
- Nguyên nhân chính: Isoniazid
- Xử trí: Tăng liều Pyridoxine lên 100 mg/ngày
3.5.4. Rối loạn thị giác
- Nguyên nhân: Ethambutol
- Xử trí: Ngưng Ethambutol ngay, chuyển khám chuyên khoa mắt
3.5.5. Đau khớp
- Nguyên nhân chính: Pyrazinamide
- Xử trí: Giảm liều Pyrazinamide, dùng NSAIDs
3.6. Điều trị trong các trường hợp đặc biệt
3.6.1. Lao và HIV
- Bắt đầu điều trị ARV sau 2-8 tuần điều trị lao
- Điều chỉnh tương tác thuốc giữa Rifampicin và ARV
3.6.2. Lao ở phụ nữ mang thai
- Tránh dùng Streptomycin
- Bổ sung Pyridoxine 50 mg/ngày
3.6.3. Lao ở bệnh nhân suy thận
- Điều chỉnh liều Ethambutol, Pyrazinamide theo mức lọc cầu thận
- Tránh dùng Streptomycin nếu có thể
3.6.4. Lao ở trẻ em
- Liều thuốc dựa trên cân nặng
- Ưu tiên dùng thuốc phối hợp liều cố định dạng hòa tan
3.7. Tiêu chuẩn khỏi bệnh
- Hoàn thành đủ liệu trình điều trị
- Xét nghiệm đờm âm tính ít nhất 2 lần vào cuối điều trị
- Cải thiện lâm sàng và X-quang
3.8. Tư vấn và hỗ trợ tuân thủ điều trị
- Giáo dục bệnh nhân về tầm quan trọng của tuân thủ điều trị
- Sử dụng các công cụ nhắc nhở (ví dụ: ứng dụng điện thoại, hộp đựng thuốc có báo giờ)
- Hỗ trợ tâm lý và xã hội
- Theo dõi chặt chẽ và can thiệp kịp thời nếu bệnh nhân bỏ trị
4. Dự phòng
4.1. Dự phòng lây nhiễm
- Cách ly bệnh nhân lao phổi AFB (+) trong 2 tuần đầu điều trị
- Đeo khẩu trang, che miệng khi ho
- Thông gió, khử trùng môi trường
4.2. Dự phòng phát bệnh
- Điều trị dự phòng cho người tiếp xúc gần:
- Isoniazid 300 mg/ngày trong 6-9 tháng
- Hoặc Isoniazid + Rifapentine hàng tuần trong 3 tháng
4.3. Tiêm chủng BCG
- Tiêm cho trẻ sơ sinh trong tháng đầu sau sinh
- Hiệu quả phòng lao nặng ở trẻ em: 60-80%
5. Quản lý và theo dõi
5.1. Đăng ký và báo cáo
- Đăng ký bệnh nhân vào hệ thống quản lý lao quốc gia
- Báo cáo định kỳ theo quy định
5.2. Tư vấn và hỗ trợ
- Tư vấn về bệnh, điều trị và phòng ngừa
- Hỗ trợ tâm lý, dinh dưỡng và xã hội
5.3. Theo dõi sau điều trị
- Khám định kỳ 3 tháng/lần trong năm đầu sau khi kết thúc điều trị
- Hướng dẫn tái khám khi có triệu chứng nghi ngờ
Tài liệu tham khảo
- World Health Organization. WHO consolidated guidelines on tuberculosis. Module 4: Treatment – Drug-resistant tuberculosis treatment. Geneva: World Health Organization; 2020.
- Centers for Disease Control and Prevention. Core Curriculum on Tuberculosis: What the Clinician Should Know. Sixth Edition. 2013.
- Nahid P, et al. Official American Thoracic Society/Centers for Disease Control and Prevention/Infectious Diseases Society of America Clinical Practice Guidelines: Treatment of Drug-Susceptible Tuberculosis. Clin Infect Dis. 2016;63(7):e147-e195.
- Hướng dẫn chẩn đoán, điều trị và dự phòng bệnh lao. Bộ Y tế Việt Nam. 2020.
- Global Tuberculosis Report 2021. World Health Organization. 2021.


BÌNH LUẬN