Phác đồ chẩn đoán và điều trị đái tháo đường trên bệnh nhân xơ gan
Ths.Bs. Lê Đình Sáng
1. Đại cương
1.1. Định nghĩa
Đái tháo đường (ĐTĐ) trên bệnh nhân xơ gan là tình trạng rối loạn chuyển hóa glucose xảy ra ở những người mắc xơ gan, bao gồm:
- ĐTĐ type 2 sẵn có trên nền xơ gan
- ĐTĐ do gan (Hepatogenous Diabetes): rối loạn chuyển hóa glucose phát sinh do tổn thương gan mạn tính
1.2. Dịch tễ học
- Tỷ lệ mắc: 30-70% bệnh nhân xơ gan có ĐTĐ hoặc rối loạn dung nạp glucose
- Phân bố:
- Giới: Nam giới có tỷ lệ mắc cao hơn (60% so với 40% ở nữ)
- Tuổi: Tăng theo độ tuổi, đặc biệt sau 50 tuổi
- Yếu tố nguy cơ chính:
- Mức độ nặng của xơ gan (Child-Pugh C > B > A)

Tiêu chí phân loại xơ gan theo thang đánh giá Child-Pugh A B C
-
- Nguyên nhân xơ gan (Viêm gan virus C > Rượu > NAFLD > Viêm gan virus B)
- Béo phì (BMI > 25 kg/m2)
- Tiền sử gia đình có ĐTĐ
- Hội chứng chuyển hóa
1.3. Sinh lý bệnh
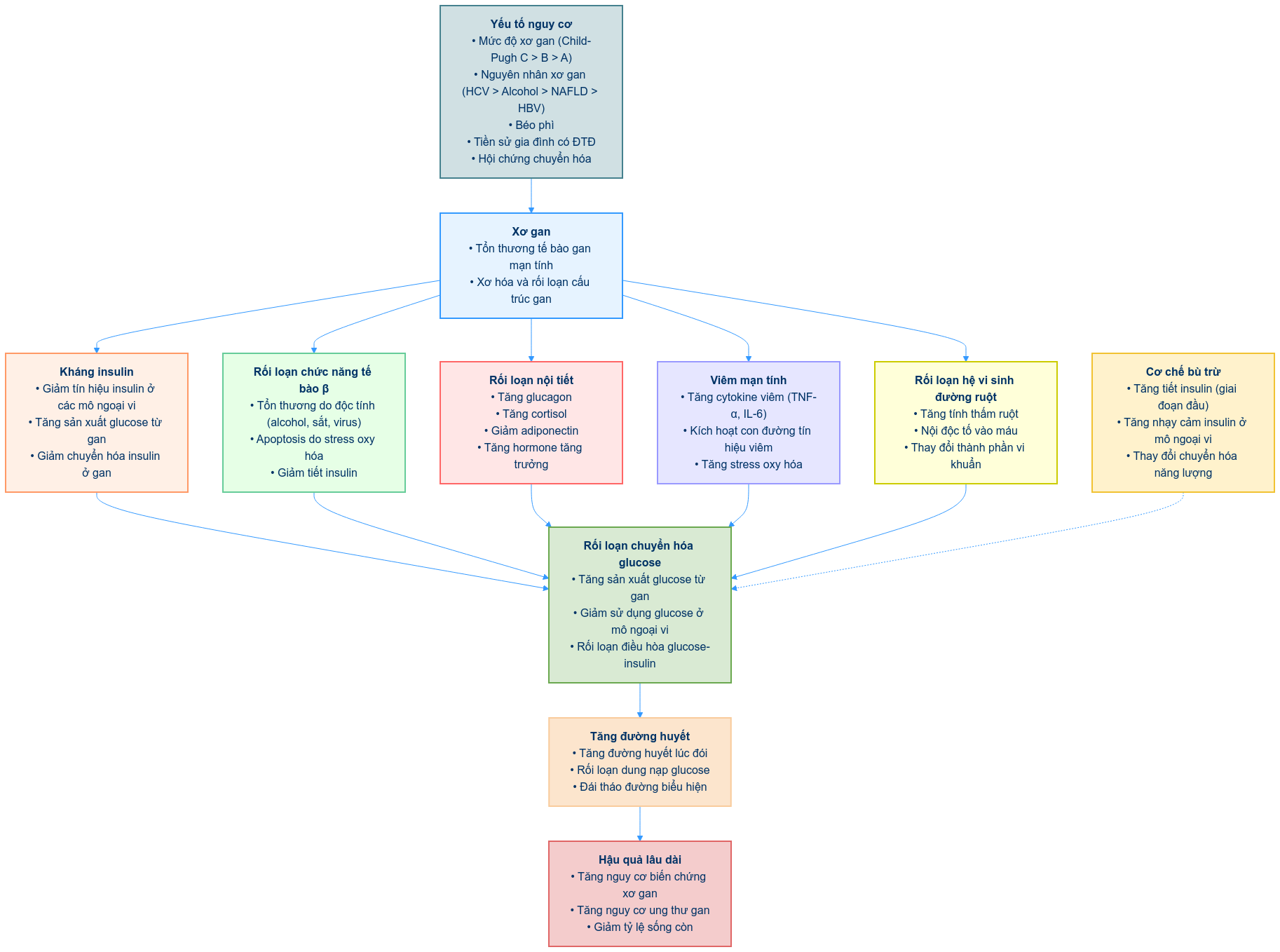
Cơ chế sinh lý bệnh của đái tháo đường trên bệnh nhân xơ gan khá phức tạp, có thể tóm lược như sau:
- Kháng insulin:
- Giảm tín hiệu insulin ở các mô ngoại vi
- Tăng sản xuất glucose từ gan
- Giảm tiết insulin:
- Tổn thương tế bào β tuyến tụy do độc tính của alcohol, sắt, virus viêm gan C
- Chết tế bào theo chương trình (Apoptosis) của tế bào β do stress oxy hóa và viêm mạn tính
- Giảm chuyển hóa insulin ở gan:
- Giảm độ thanh thải insulin do shunt cửa chủ và giảm chức năng gan
- Tăng nồng độ các cytokine gây viêm:
- TNF-α, IL-6 làm tăng kháng insulin
- Rối loạn trục gan-ruột và hệ vi sinh đường ruột:
- Tăng tính thấm ruột, nội độc tố vào máu
- Thay đổi thành phần vi khuẩn đường ruột ảnh hưởng đến chuyển hóa glucose
- Thay đổi nồng độ các hormone:
- Tăng glucagon, cortisol
- Giảm adiponectin
1.4. Phân loại
- ĐTĐ type 2 trên nền xơ gan:
- ĐTĐ xuất hiện trước hoặc đồng thời với xơ gan
- Thường liên quan đến béo phì, hội chứng chuyển hóa
- ĐTĐ do gan (Hepatogenous Diabetes):
- Phát sinh sau khi xơ gan đã được chẩn đoán
- Thường không có tiền sử gia đình ĐTĐ
- Có thể hồi phục sau ghép gan
2. Chẩn đoán
2.1. Lâm sàng
- Triệu chứng:
- Đa số không có triệu chứng đặc hiệu
- Có thể gặp: khát nước, tiểu nhiều, sụt cân không rõ nguyên nhân
- Triệu chứng có thể bị che lấp bởi biểu hiện của xơ gan
- Dấu hiệu:
- Các dấu hiệu của xơ gan: bụng chướng, lòng bàn tay đỏ, sao mạch, tuần hoàn bàng hệ
- Dấu hiệu của biến chứng ĐTĐ (nếu có): bệnh lý võng mạc, bệnh thận ĐTĐ
2.2. Cận lâm sàng
2.2.1. Xét nghiệm đường huyết
a) Đường huyết lúc đói (FPG):
- Định nghĩa: ≥ 8 giờ không ăn
- Tiêu chuẩn: ≥ 126 mg/dL (7.0 mmol/L) trong 2 lần xét nghiệm
- Ưu điểm: Đơn giản, rẻ tiền
- Nhược điểm: Có thể âm tính giả ở bệnh nhân xơ gan do giảm dự trữ glycogen
b) Đường huyết ngẫu nhiên:
- Tiêu chuẩn: ≥ 200 mg/dL (11.1 mmol/L) kèm triệu chứng ĐTĐ điển hình
- Ưu điểm: Nhanh, không cần chuẩn bị
- Nhược điểm: Độ nhạy thấp
c) HbA1c:
- Tiêu chuẩn: ≥ 6.5%
- Ưu điểm: Phản ánh kiểm soát đường huyết trong 2-3 tháng
- Nhược điểm ở bệnh nhân xơ gan:
- Giảm giá trị do thiếu máu, tăng bilirubin, tăng urê huyết
- Tăng giá trị do tăng carbamylated hemoglobin trong suy thận
2.2.2. Nghiệm pháp dung nạp glucose đường uống (OGTT)
- Quy trình:
- Nhịn đói 8-12 giờ
- Uống 75g glucose hòa tan trong 300ml nước
- Đo đường huyết tại thời điểm 0 và 2 giờ sau uống
- Tiêu chuẩn chẩn đoán:
- Đường huyết sau 2 giờ ≥ 200 mg/dL (11.1 mmol/L)
- Ưu điểm:
- Độ nhạy và độ đặc hiệu cao nhất ở bệnh nhân xơ gan
- Phát hiện sớm rối loạn dung nạp glucose
- Nhược điểm:
- Tốn thời gian, khó thực hiện ở bệnh nhân ngoại trú
2.2.3. Đánh giá chức năng gan
a) Xét nghiệm sinh hóa:
- ALT, AST: đánh giá tổn thương tế bào gan
- Bilirubin: đánh giá chức năng bài tiết của gan
- Albumin: đánh giá chức năng tổng hợp của gan
- INR (International Normalized Ratio): đánh giá đông máu
b) Child-Pugh score:
- Thang điểm đánh giá mức độ nặng của xơ gan
- Tiêu chí: Bilirubin, Albumin, INR, Cổ trướng, Bệnh não gan
- Phân loại:
- Child-Pugh A: 5-6 điểm
- Child-Pugh B: 7-9 điểm
- Child-Pugh C: 10-15 điểm
c) MELD score (Model for End-Stage Liver Disease):
- Công thức tính: 3.78×ln[bilirubin (mg/dL)] + 11.2×ln[INR] + 9.57×ln[creatinine (mg/dL)] + 6.43
- Dùng để đánh giá tiên lượng và ưu tiên ghép gan
d) Các xét nghiệm khác:
- Siêu âm gan: đánh giá cấu trúc gan, tình trạng cổ trướng
- FibroScan: đánh giá mức độ xơ hóa gan
- Nội soi thực quản: đánh giá giãn tĩnh mạch thực quản
2.3. Chẩn đoán xác định
- Dựa trên tiêu chuẩn chẩn đoán ĐTĐ của ADA (American Diabetes Association):
- FPG ≥ 126 mg/dL (7.0 mmol/L), hoặc
- Đường huyết sau 2 giờ trong OGTT ≥ 200 mg/dL (11.1 mmol/L), hoặc
- HbA1c ≥ 6.5%, hoặc
- Đường huyết ngẫu nhiên ≥ 200 mg/dL (11.1 mmol/L) kèm triệu chứng ĐTĐ điển hình
- Cần loại trừ các nguyên nhân gây tăng đường huyết tạm thời:
- Nhiễm trùng cấp tính
- Sử dụng thuốc corticosteroid
- Stress do nhập viện
2.4. Chẩn đoán phân biệt
- ĐTĐ type 1:
- Thường khởi phát đột ngột, ở người trẻ tuổi
- Có thể có ketoacidosis (nhiễm toan ceton)
- Xét nghiệm kháng thể GAD, IA-2, IAA dương tính
- Tăng đường huyết do stress:
- Thường xảy ra trong bệnh cảnh cấp tính (nhiễm trùng, phẫu thuật)
- Đường huyết trở về bình thường sau khi tình trạng cấp tính được giải quyết
- Rối loạn dung nạp glucose:
- Đường huyết sau 2 giờ trong OGTT: 140-199 mg/dL (7.8-11.0 mmol/L)
- Cần theo dõi và can thiệp sớm để ngăn ngừa tiến triển thành ĐTĐ
3. Điều trị
3.1. Nguyên tắc điều trị
- Kiểm soát đường huyết để ngăn ngừa biến chứng cấp và mạn tính của ĐTĐ
- Cân nhắc nguy cơ hạ đường huyết và tác dụng phụ của thuốc trên gan
- Điều trị toàn diện xơ gan và các biến chứng liên quan
- Cá thể hóa mục tiêu điều trị dựa trên tình trạng lâm sàng của bệnh nhân
- Theo dõi và điều chỉnh phác đồ điều trị thường xuyên
3.2. Điều trị cụ thể
3.2.1. Thay đổi lối sống
a) Chế độ ăn:
- Hạn chế natri: < 2g/ngày để kiểm soát cổ trướng
- Protein: 0.8-1.2g/kg/ngày (tùy mức độ xơ gan và nguy cơ bệnh não gan)
- Carbohydrate:
- Ưu tiên carbohydrate phức hợp, chỉ số đường huyết thấp
- 50-60% tổng năng lượng
- Chất béo: 25-35% tổng năng lượng, ưu tiên chất béo không bão hòa
- Hạn chế rượu bia tuyệt đối
b) Tập luyện:
- Vận động nhẹ nhàng: đi bộ, bơi lội, yoga
- Thời gian: 30 phút/ngày, 5 ngày/tuần
- Tránh gắng sức quá mức, đặc biệt ở bệnh nhân có giãn tĩnh mạch thực quản
c) Kiểm soát cân nặng:
- Mục tiêu: BMI 18.5-24.9 kg/m2
- Giảm cân từ từ: 0.5-1 kg/tuần ở bệnh nhân thừa cân, béo phì
3.2.2. Điều trị nội khoa
a) Metformin:
- Cơ chế tác dụng: Giảm sản xuất glucose ở gan, tăng nhạy cảm insulin
- Chỉ định: Xơ gan Child-Pugh A
- Liều dùng:
- Bắt đầu: 500mg/ngày, uống cùng bữa ăn
- Tăng dần: 500mg mỗi tuần
- Liều tối đa: 1000mg x 2 lần/ngày
- Chống chỉ định: Child-Pugh B, C; eGF
b) Sulfonylureas:
- Cơ chế tác dụng: Kích thích tiết insulin từ tế bào β tuyến tụy
- Chỉ định: Hạn chế sử dụng do nguy cơ hạ đường huyết cao
- Có thể cân nhắc Gliclazide ở bệnh nhân Child-Pugh A
- Liều dùng Gliclazide:
- Bắt đầu: 30-60mg/ngày
- Tăng dần: 30mg mỗi 2 tuần nếu cần
- Liều tối đa: 120mg/ngày
- Chống chỉ định: Child-Pugh B, C; suy thận nặng
- Theo dõi: Nguy cơ hạ đường huyết, chức năng gan và thận
c) Thuốc ức chế DPP-4:
- Cơ chế tác dụng: Ức chế enzyme phân hủy GLP-1, tăng tiết insulin phụ thuộc glucose
- An toàn và hiệu quả ở bệnh nhân xơ gan
- Các thuốc và liều dùng:
- Linagliptin: 5mg/ngày, không cần điều chỉnh liều ở bệnh nhân xơ gan và suy thận
- Sitagliptin: 100mg/ngày (điều chỉnh liều theo mức lọc cầu thận)
- Vildagliptin: 50mg x 2 lần/ngày (thận trọng ở bệnh nhân có men gan tăng)
- Ưu điểm: Ít tác dụng phụ, không gây hạ đường huyết
- Theo dõi: Chức năng gan định kỳ
d) Thuốc chủ vận thụ thể GLP-1 (GLP-1 receptor agonists):
- Cơ chế tác dụng: Kích thích thụ thể GLP-1, tăng tiết insulin phụ thuộc glucose, giảm tiết glucagon
- Chỉ định: Cân nhắc sử dụng ở bệnh nhân béo phì, xơ gan còn bù
- Các thuốc và liều dùng:
- Liraglutide: bắt đầu 0.6mg/ngày, tăng dần tới 1.8mg/ngày sau 1-2 tuần
- Semaglutide: bắt đầu 0.25mg/tuần, tăng dần tới 1mg/tuần sau 4 tuần
- Ưu điểm: Giảm cân, cải thiện lipid máu, có thể làm chậm tiến triển xơ gan
- Theo dõi: Tác dụng phụ trên đường tiêu hóa, nguy cơ viêm tụy cấp
e) Insulin:
- Chỉ định:
- ĐTĐ không kiểm soát được bằng thuốc uống:
- HbA1c > 9% sau 3 tháng điều trị tối ưu bằng thuốc uống
- Đường huyết lúc đói > 250 mg/dL hoặc đường huyết ngẫu nhiên > 300 mg/dL kéo dài
- Có triệu chứng tăng đường huyết rõ rệt (đa niệu, đa uống, sụt cân)
- Xơ gan tiến triển:
- Child-Pugh B hoặc C
- Bilirubin > 2 mg/dL hoặc INR > 1.5
- Có biến chứng của xơ gan như cổ trướng, bệnh não gan
- ĐTĐ mới chẩn đoán có triệu chứng rõ rệt hoặc đường huyết rất cao (> 300 mg/dL)
- Trước, trong và sau các thủ thuật hoặc phẫu thuật
- Trong các tình trạng cấp tính: nhiễm trùng, xuất huyết tiêu hóa
- ĐTĐ không kiểm soát được bằng thuốc uống:
- Liều dùng và cách tiếp cận cá nhân hóa:
a) Nguyên tắc chung:
- Bắt đầu với liều thấp: 0.1-0.2 đơn vị/kg/ngày
- Tăng liều từ từ: 10-15% mỗi 3-4 ngày dựa trên đường huyết
- Mục tiêu đường huyết:
- Lúc đói và trước bữa ăn: 80-130 mg/dL
- 2 giờ sau ăn: < 180 mg/dL
- Điều chỉnh liều dựa trên chức năng gan và thận
b) Phác đồ insulin cụ thể:
i. Phác đồ Basal (insulin nền):
- Chỉ định: Đường huyết lúc đói cao, kiểm soát đường huyết không quá kém
- Insulin sử dụng: Glargine, Detemir, NPH
- Liều khởi đầu: 0.1-0.2 đơn vị/kg, tiêm dưới da 1 lần/ngày (thường vào buổi tối)
- Điều chỉnh: Tăng/giảm 10-15% mỗi 3-4 ngày dựa trên đường huyết lúc đói
ii. Phác đồ Basal-Bolus:
- Chỉ định: Kiểm soát đường huyết kém, đường huyết dao động nhiều
- Insulin sử dụng:
- Basal: Glargine, Detemir
- Bolus: Aspart, Lispro, Regular (trước bữa ăn)
- Liều khởi đầu: Tổng 0.3-0.5 đơn vị/kg/ngày, chia như sau:
- 50% liều basal
- 50% liều bolus, chia đều cho 3 bữa ăn chính
- Điều chỉnh:
- Basal: dựa trên đường huyết lúc đói
- Bolus: dựa trên đường huyết trước bữa ăn và 2 giờ sau ăn
iii. Phác đồ Premixed insulin:
- Chỉ định: Bệnh nhân có lịch sinh hoạt đều đặn, khó thực hiện nhiều mũi tiêm
- Insulin sử dụng: 70/30 hoặc 75/25 (NPH/Regular hoặc NPH/Analog)
- Liều khởi đầu: 0.2-0.3 đơn vị/kg/ngày, chia 2 lần (trước bữa sáng và bữa tối)
- Điều chỉnh: 10-15% mỗi 3-4 ngày dựa trên đường huyết trước bữa ăn và 2 giờ sau ăn
c) Cách tiếp cận cá nhân hóa:
i. Dựa trên mức độ xơ gan:
- Child-Pugh A: Có thể sử dụng tất cả các loại insulin
- Child-Pugh B: Ưu tiên insulin analog (Glargine, Detemir, Aspart, Lispro) do ít nguy cơ hạ đường huyết
- Child-Pugh C: Sử dụng insulin analog, giảm liều 25-50%, theo dõi sát
ii. Dựa trên chức năng thận:
- eGFR > 50 ml/min: Không cần điều chỉnh liều
- eGFR 30-50 ml/min: Giảm liều 25%
- eGFR < 30 ml/min: Giảm liều 50%, theo dõi sát
iii. Dựa trên tình trạng dinh dưỡng:
- Suy dinh dưỡng: Bắt đầu với liều thấp hơn (0.1 đơn vị/kg/ngày), tăng liều chậm
- Béo phì: Có thể cần liều cao hơn, tính liều dựa trên cân nặng lý tưởng
iv. Điều chỉnh theo tình trạng cụ thể:
- Nhiễm trùng/Stress: Tăng liều tạm thời 20-30%
- Giảm ăn/Nôn: Giảm liều 20-30%, theo dõi sát nguy cơ hạ đường huyết
- Sử dụng corticosteroid: Tăng liều insulin 20-40%, đặc biệt là insulin tác dụng nhanh
- Theo dõi và điều chỉnh:
- Đường huyết mao mạch: 3-4 lần/ngày (trước bữa ăn và trước khi ngủ)
- HbA1c: mỗi 3 tháng
- Điều chỉnh liều mỗi 3-4 ngày cho đến khi đạt mục tiêu
- Đánh giá lại phác đồ insulin mỗi 2-4 tuần trong giai đoạn đầu, sau đó mỗi 3 tháng
- Lưu ý đặc biệt:
- Giáo dục bệnh nhân về kỹ thuật tiêm insulin, nhận biết và xử trí hạ đường huyết
- Cung cấp glucagon cho người nhà bệnh nhân sử dụng khi có hạ đường huyết nặng
- Điều chỉnh liều insulin khi có thay đổi về chế độ ăn, mức độ hoạt động thể chất, hoặc tình trạng bệnh gan
- Cân nhắc chuyển sang bơm insulin ở bệnh nhân khó kiểm soát đường huyết hoặc có nhiều biến động
- Theo dõi tác dụng không mong muốn:
- Hạ đường huyết: Nguy cơ cao ở bệnh nhân xơ gan, đặc biệt là Child-Pugh B và C
- Tăng cân: Có thể làm nặng thêm tình trạng cổ trướng
- Phù: Theo dõi ở bệnh nhân có nguy cơ suy tim
- Lipodystrophy: Hướng dẫn bệnh nhân thay đổi vị trí tiêm
Việc sử dụng insulin ở bệnh nhân đái tháo đường kèm xơ gan đòi hỏi sự theo dõi sát và điều chỉnh linh hoạt. Cần cân nhắc cẩn thận giữa lợi ích của việc kiểm soát đường huyết và nguy cơ hạ đường huyết, đặc biệt ở những bệnh nhân xơ gan tiến triển.
3.3. Điều trị theo mức độ xơ gan
a) Child-Pugh A:
- Ưu tiên: Metformin, DPP-4 inhibitors
- Cân nhắc: GLP-1 RAs nếu béo phì
- Theo dõi chặt chẽ chức năng gan và thận
b) Child-Pugh B:
- Ưu tiên: DPP-4 inhibitors, Insulin
- Tránh sử dụng Metformin và Sulfonylureas
- Điều chỉnh liều thuốc theo chức năng gan
c) Child-Pugh C:
- Ưu tiên: Insulin
- Cân nhắc: DPP-4 inhibitors ở liều thấp
- Theo dõi sát nguy cơ hạ đường huyết
3.4. Theo dõi và đánh giá
a) Mục tiêu kiểm soát đường huyết:
- HbA1c: < 7% (có thể nới lỏng 7-8% ở bệnh nhân xơ gan nặng)
- Đường huyết lúc đói: 80-130 mg/dL
- Đường huyết sau ăn 2 giờ: < 180 mg/dL
b) Tần suất theo dõi:
- Đường huyết mao mạch: Hàng ngày ở bệnh nhân nội trú, 2-3 lần/tuần ở bệnh nhân ngoại trú ổn định
- HbA1c: 3 tháng/lần (lưu ý giá trị có thể không chính xác ở bệnh nhân thiếu máu nặng)
- Chức năng gan: ALT, AST, Bilirubin, Albumin, INR mỗi 3-6 tháng
- Siêu âm gan: 6 tháng/lần để đánh giá tiến triển xơ gan và sàng lọc ung thư gan
- Nội soi thực quản: 1-2 năm/lần để đánh giá giãn tĩnh mạch thực quản
c) Đánh giá biến chứng:
- Biến chứng ĐTĐ:
- Bệnh thận: Microalbumin niệu, creatinine huyết thanh hàng năm
- Bệnh võng mạc: Khám mắt hàng năm
- Bệnh thần kinh: Khám lâm sàng hàng năm
- Biến chứng xơ gan:
- Cổ trướng: Khám lâm sàng và siêu âm định kỳ
- Bệnh não gan: Đánh giá trạng thái tâm thần và các test thần kinh đơn giản
- Nhiễm trùng: Cảnh giác với các dấu hiệu nhiễm trùng, đặc biệt viêm phúc mạc nhiễm khuẩn tự phát
d) Điều chỉnh phác đồ điều trị:
- Đánh giá hiệu quả và tác dụng phụ của thuốc mỗi 3 tháng
- Điều chỉnh liều hoặc thay đổi thuốc nếu không đạt mục tiêu hoặc có tác dụng phụ
- Cân nhắc chuyển sang insulin sớm nếu kiểm soát đường huyết kém
4. Tiên lượng
a) Yếu tố tiên lượng xấu:
- Xơ gan tiến triển (Child-Pugh B, C)
- Kiểm soát đường huyết kém (HbA1c > 8%)
- Biến chứng xơ gan: cổ trướng khó kiểm soát, bệnh não gan tái phát
- Suy dinh dưỡng nặng
- Nhiễm trùng tái phát
b) Yếu tố tiên lượng tốt:
- Xơ gan còn bù (Child-Pugh A)
- Kiểm soát đường huyết tốt (HbA1c < 7%)
- Không có biến chứng nặng của xơ gan
- Tuân thủ điều trị và chế độ ăn uống
c) Tác động của ĐTĐ lên tiên lượng xơ gan:
- Tăng nguy cơ biến chứng xơ gan (cổ trướng, xuất huyết tiêu hóa)
- Tăng nguy cơ ung thư gan nguyên phát
- Giảm tỷ lệ sống còn sau 5 năm
d) Khả năng hồi phục:
- ĐTĐ do gan có thể cải thiện sau ghép gan thành công
- Cải thiện kiểm soát đường huyết có thể làm chậm tiến triển của xơ gan
5. Phòng bệnh
a) Kiểm soát tốt các yếu tố nguy cơ:
- Hạn chế sử dụng rượu bia
- Kiểm soát cân nặng, điều trị béo phì
- Điều trị viêm gan virus (B, C) tích cực
b) Tầm soát ĐTĐ định kỳ ở bệnh nhân xơ gan:
- OGTT hàng năm ở bệnh nhân xơ gan chưa có ĐTĐ
- Đánh giá HbA1c, đường huyết lúc đói mỗi 6 tháng
c) Giáo dục bệnh nhân:
- Nhận biết triệu chứng ĐTĐ và biến chứng xơ gan
- Tầm quan trọng của chế độ ăn uống và lối sống lành mạnh
- Kỹ năng tự theo dõi đường huyết tại nhà
d) Quản lý toàn diện:
- Phối hợp giữa bác sĩ nội tiết, gan mật và dinh dưỡng
- Tư vấn tâm lý hỗ trợ
e) Nghiên cứu và phát triển:
- Tìm hiểu cơ chế bệnh sinh của ĐTĐ trên bệnh nhân xơ gan
- Phát triển các phương pháp điều trị mới, an toàn và hiệu quả hơn
6. Thách thức và cạm bẫy trong chẩn đoán, điều trị và quản lý đái tháo đường ở bệnh nhân xơ gan
6.1. Thách thức trong chẩn đoán
- Độ tin cậy của các xét nghiệm thông thường:
- HbA1c: Có thể không đáng tin cậy do:
- Thiếu máu (phổ biến ở bệnh nhân xơ gan)
- Tăng bilirubin làm ảnh hưởng đến kết quả xét nghiệm
- Tăng tốc độ thay thế hồng cầu do cường lách
- Đường huyết lúc đói: Có thể bị ảnh hưởng bởi:
- Giảm dự trữ glycogen ở gan
- Rối loạn chuyển hóa glucose do suy giảm chức năng gan
- HbA1c: Có thể không đáng tin cậy do:
- Triệu chứng chồng chéo:
- Mệt mỏi, sụt cân, và đa niệu có thể do xơ gan hoặc đái tháo đường
- Khó phân biệt giữa bệnh não gan và hạ đường huyết
- Rối loạn dung nạp glucose tạm thời:
- Nhiễm trùng hoặc stress có thể gây tăng đường huyết tạm thời
- Khó phân biệt với đái tháo đường thực sự
- Thiếu các tiêu chuẩn chẩn đoán cụ thể:
- Tiêu chuẩn chẩn đoán đái tháo đường hiện tại có thể không phù hợp hoàn toàn cho bệnh nhân xơ gan
6.2. Thách thức trong điều trị
- Lựa chọn thuốc:
- Hầu hết các thuốc điều trị đái tháo đường đều chuyển hóa qua gan
- Nguy cơ tích lũy thuốc và tác dụng phụ ở bệnh nhân suy gan
- Nguy cơ hạ đường huyết:
- Tăng nguy cơ do giảm dự trữ glycogen và suy giảm gluconeogenesis
- Khó phát hiện vì triệu chứng có thể bị che lấp bởi bệnh não gan
- Quản lý insulin:
- Kháng insulin phổ biến ở bệnh nhân xơ gan
- Nhu cầu insulin có thể thay đổi nhanh chóng theo tình trạng gan
- Tương tác thuốc:
- Nhiều tương tác giữa thuốc điều trị đái tháo đường và thuốc điều trị xơ gan
- Ví dụ: Beta-blocker (điều trị tăng áp lực tĩnh mạch cửa) có thể che lấp triệu chứng hạ đường huyết
- Kiểm soát cân nặng:
- Khó khăn trong việc đánh giá cân nặng thực do cổ trướng
- Mâu thuẫn giữa nhu cầu giảm cân (với ĐTĐ type 2) và duy trì dinh dưỡng (với xơ gan)
- Điều trị ở bệnh nhân nghiện rượu:
- Khó kiểm soát đường huyết do tiếp tục sử dụng rượu
- Nguy cơ cao của hạ đường huyết khi ngưng rượu đột ngột
6.3. Thách thức trong quản lý lâu dài
- Theo dõi biến chứng:
- Khó phân biệt giữa biến chứng của đái tháo đường và xơ gan
- Ví dụ: Bệnh thận do đái tháo đường vs. Hội chứng gan thận
- Quản lý dinh dưỡng:
- Mâu thuẫn giữa chế độ ăn cho đái tháo đường (hạn chế carbohydrate) và xơ gan (đủ carbohydrate để ngăn ngừa tiêu hủy protein)
- Tuân thủ điều trị:
- Phức tạp do nhiều loại thuốc và chế độ điều trị
- Khó khăn trong việc tự theo dõi đường huyết ở bệnh nhân bệnh não gan
- Quản lý trong các tình huống đặc biệt:
- Xuất huyết tiêu hóa: Cần điều chỉnh nhanh chóng liều insulin
- Nhiễm trùng: Tăng đột biến nhu cầu insulin
- Thủ thuật/phẫu thuật: Cần cân nhắc cẩn thận việc nhịn ăn và điều chỉnh thuốc
- Ghép gan:
- Khó dự đoán sự thay đổi của tình trạng đái tháo đường sau ghép gan
- Tác động của thuốc ức chế miễn dịch lên kiểm soát đường huyết
- Giáo dục bệnh nhân:
- Khó khăn trong việc truyền đạt thông tin phức tạp cho bệnh nhân, đặc biệt khi có bệnh não gan
- Phối hợp đa chuyên khoa:
- Cần sự phối hợp chặt chẽ giữa bác sĩ nội tiết, gan mật, dinh dưỡng
- Có thể có mâu thuẫn trong cách tiếp cận điều trị giữa các chuyên khoa
6.4. Cạm bẫy thường gặp
- Đánh giá thấp nguy cơ hạ đường huyết:
- Cần nhận thức rằng nguy cơ hạ đường huyết cao hơn nhiều ở bệnh nhân xơ gan
- Phụ thuộc quá mức vào HbA1c:
- Cần sử dụng nhiều phương pháp đánh giá kiểm soát đường huyết khác nhau
- Bỏ qua tầm quan trọng của chế độ ăn:
- Chế độ ăn đóng vai trò quan trọng trong kiểm soát cả đái tháo đường và xơ gan
- Điều trị quá tích cực:
- Mục tiêu đường huyết quá thấp có thể gây hại nhiều hơn lợi ở bệnh nhân xơ gan tiến triển
- Bỏ qua các yếu tố tâm lý xã hội:
- Trầm cảm và lo âu phổ biến ở bệnh nhân mắc cả hai bệnh, ảnh hưởng đến kết quả điều trị
- Không điều chỉnh liều thuốc kịp thời:
- Tình trạng gan có thể thay đổi nhanh chóng, đòi hỏi điều chỉnh liều thường xuyên
- Bỏ qua tầm quan trọng của tầm soát ung thư gan:
- Đái tháo đường là yếu tố nguy cơ độc lập của ung thư gan ở bệnh nhân xơ gan
6.5. Chiến lược khắc phục
- Sử dụng phương pháp chẩn đoán tổng hợp:
- Kết hợp nhiều phương pháp đánh giá đường huyết (đường huyết lúc đói, sau ăn, HbA1c, fructosamine)
- Cá nhân hóa mục tiêu điều trị:
- Điều chỉnh mục tiêu HbA1c dựa trên mức độ xơ gan và nguy cơ hạ đường huyết
- Tối ưu hóa chế độ dinh dưỡng:
- Phối hợp với chuyên gia dinh dưỡng để cân bằng nhu cầu cho cả đái tháo đường và xơ gan
- Giáo dục bệnh nhân và người nhà:
- Đào tạo kỹ lưỡng về cách nhận biết và xử trí hạ đường huyết
- Theo dõi chặt chẽ và điều chỉnh thường xuyên:
- Đánh giá lại phác đồ điều trị mỗi 2-4 tuần trong giai đoạn đầu
- Phối hợp đa chuyên khoa:
- Tổ chức hội chẩn định kỳ giữa các chuyên khoa để thống nhất phương pháp điều trị
- Nghiên cứu và phát triển:
- Cần có thêm nghiên cứu để xây dựng hướng dẫn cụ thể cho nhóm bệnh nhân đặc biệt này
Việc nhận thức được những thách thức và cạm bẫy này sẽ giúp các bác sĩ lâm sàng tiếp cận một cách toàn diện và thận trọng hơn trong việc chẩn đoán, điều trị và quản lý đái tháo đường ở bệnh nhân xơ gan.
Tài liệu tham khảo
- American Diabetes Association. Standards of Medical Care in Diabetes-2023. Diabetes Care. 2023;46(Supplement 1).
- European Association for the Study of the Liver. EASL Clinical Practice Guidelines on nutrition in chronic liver disease. J Hepatol. 2019;70(1):172-193.
- Gundling F, et al. How to treat type 2 diabetes in patients with chronic liver disease. Digestion. 2021;102(5):746-759.
- García-Compeán D, et al. Hepatogenous diabetes: Is it a neglected condition in chronic liver disease? World J Gastroenterol. 2016;22(10):2869-2874.
- Elkrief L, et al. Diabetes mellitus in patients with cirrhosis: clinical implications and management. Liver Int. 2016;36(7):936-948.

BÌNH LUẬN